発表のポイント
- 細胞の環境への応答と寿命に重要な、出芽酵母の2種類のトア複合体は、従来手法では違いを調べる方法が無く、同一の機能を持つと考えられていた。
- 計算機を用いた構造予測を活用することで、タンパク質を合理的に改造し、片方のトア複合体のみを持つ出芽酵母を作り、機能的な違いを識別することに成功した。
- この研究は、タンパク質の機能を精密に改変することで細胞の振る舞いをより詳細に調べる手法を提供し、細胞のシグナル伝達の理解を深め、将来的には疾患治療や寿命延長に向けた新たなアプローチを可能にすると期待される。
概要
自然科学研究機構分子科学研究所/生命創成探究センター(ExCELLS)/総合研究大学院大学の小杉貴洋助教、自然科学研究機構基礎生物学研究所/総合研究大学院大学の鎌田芳彰助教、大坪瑶子研究員(現:東京大学生命科学ネットワーク)、山下朗兼任准教授(現:東京大学大学院総合文化研究科)らは、長浜バイオ大学の梅田知晴大学院生、向由起夫教授、名古屋大学の大塚北斗助教らと共同で、出芽酵母のトア複合体を改造することにより、これまで同じ機能を持つと考えられていた2種類のトア複合体が異なる働きを持つことを明らかにしました。
本研究の成果は、「Journal of Cell Science」に2024年2月28日付で公開されました。
研究の背景
生体内には、いくつものタンパク質が集まって会合したタンパク質複合体が多数存在し、重要な役割を果たしています。一般的に、タンパク質複合体は、共通するタンパク質を含んでいても、その他の構成タンパク質が変わると、その機能も変わります。生物は、構成タンパク質の組み合わせが異なる複合体を巧みに利用することで、生体内の複雑なシステムの制御を行っています。
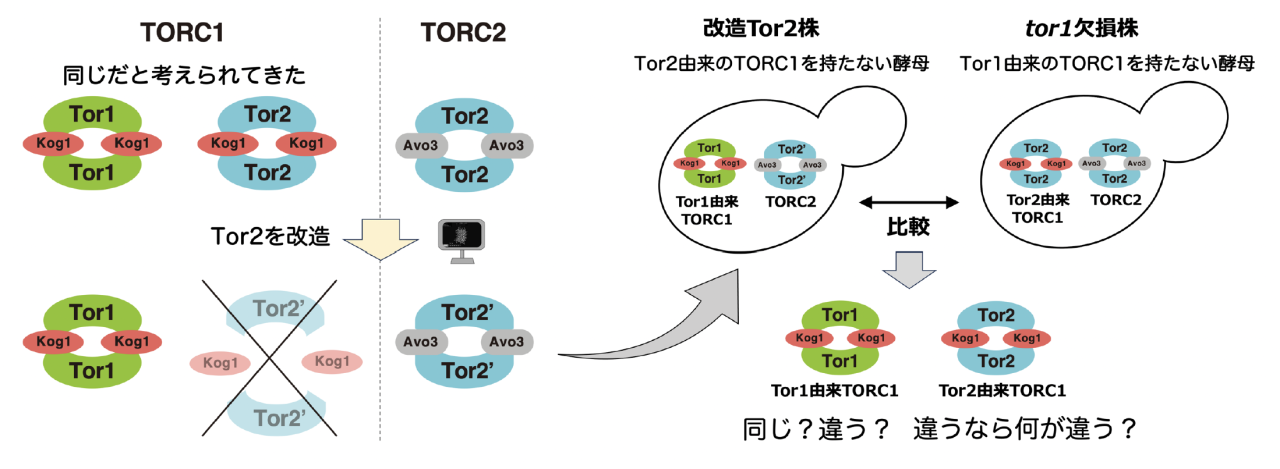
細胞の環境への応答に不可欠であり細胞寿命に関わっているタンパク質複合体であるTarget of Rapamycin (TOR、トア)複合体(1)にも、TORC1とTORC2という構成タンパク質の組み合わせが異なる複合体状態が存在し、それぞれ異なる機能を持っていることがわかっています。さらに、分裂酵母や哺乳類はTORC1を1種類しか持っていませんが、出芽酵母(2)には構成タンパク質の異なる2種類のTORC1を持っていることが知られています(図1)。しかし、これまで出芽酵母の2種類のTORC1の違いを調べる手段がなかったため、これらが比較され機能的な違いがあるのかは明らかにされていませんでした。それにもかかわらず、これらの2種類のTORC1は、これまでずっと同じ機能を持っていると考えられてきました。
近年、タンパク質構造を予測する技術やタンパク質を合理的に改造する技術が急速に発展してきました。我々は、計算機上でトア複合体の予測構造モデルを構築し、それらに基づいて合理的にタンパク質の改変を行うことにより、出芽酵母の2つのTORC1のうち一つだけを形成できなくする改造ができるのではないかと考えました。そして、その改造TORC1を用いて、2種類のTORC1のうち片方ずつしか持たない酵母を作り出すことで、二つのTORC1が同じなのか違うのか、違う場合はどのように違うのかを明らかにできると考え、研究を進めました(図1)。
研究の成果
出芽酵母はTor1とTor2という2種類のTORキナーゼ(3)をもち、Tor1とTor2の両方がKog1などの構成タンパク質と結合しTORC1になることができ、Tor2だけがAvo3などの構成タンパク質と結合しTORC2になることができます。つまり、TORC1にはTor1由来のものとTor2由来のものが存在することになります。Tor1の遺伝子を欠損させる(4)ことで、Tor1由来のTORC1だけをなくすことができ、Tor1由来のTORC1の働きが調べられてきました。特に、Tor1由来のTORC1をなくすことで、細胞の寿命が延びることが知られており、TORC1は寿命を研究するための標的として精力的に研究が行われてきました。一方で、TORC1とTORC2のどちらかが機能しなくなるだけで酵母は死んでしまうため、TORC2がなくなってしまうTor2遺伝子を欠損した酵母は生育が不可能となります。その結果、Tor2由来のTORC1だけを持たない酵母を作り出すことができず、Tor2由来のTORC1については調べられてきませんでした。それにもかかわらず、他の構成タンパク質が同じであるという理由でTor1由来のTORC1とTor2由来のTORC1は同じ働きをしていると考えられてきました。
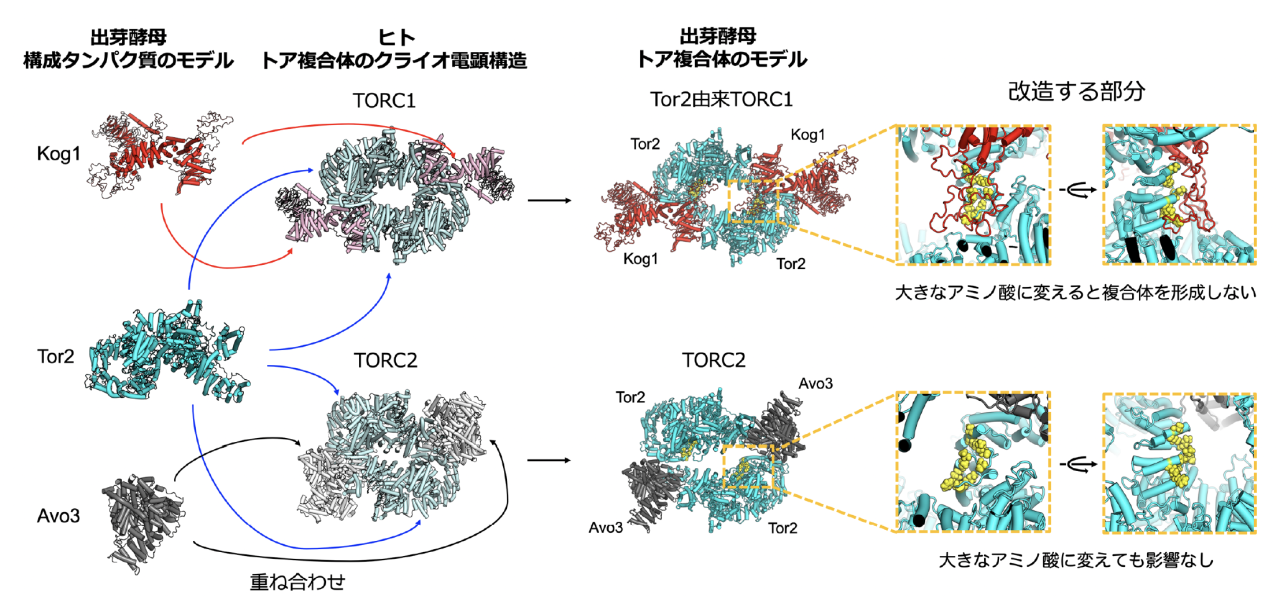
我々は、計算機上で出芽酵母トア複合体の予測構造モデルを作り、それらの予測構造に基づいてTor2を合理的に改変することにより、TORC2形成能を維持させたまま、TORC1形成能を持たない改造Tor2を作り出すことに成功しました。具体的には、ヒトのトア複合体のクライオ電顕構造を基にしてTor2由来のTORC1とTORC2のモデル構造を作りました。次に、それぞれに含まれるTor2が、TORC1ではKog1と接触していて、TORC2ではAvo3と接触していない部分を設計部位としました(図2)。そして、ここにあるいくつかのアミノ酸をより大きなものへと変え、TORC1では複合体が壊れるが、TORC2では影響がないように、Tor2を改造しました。これまでTor2由来のTORC1だけを持たない細胞を作り出すことはできませんでしたが、この新たに作られた改造Tor2によりTor1由来のTORC1は持っているが、Tor2由来のTORC1だけを持たない細胞を作り出すことに成功しました。その結果、Tor1由来のTORC1を持たない細胞とTor2由来のTORC1を持たない細胞を比べることで、Tor1由来のTORC1とTor2由来のTORC1の役割を比較することが可能になりました。
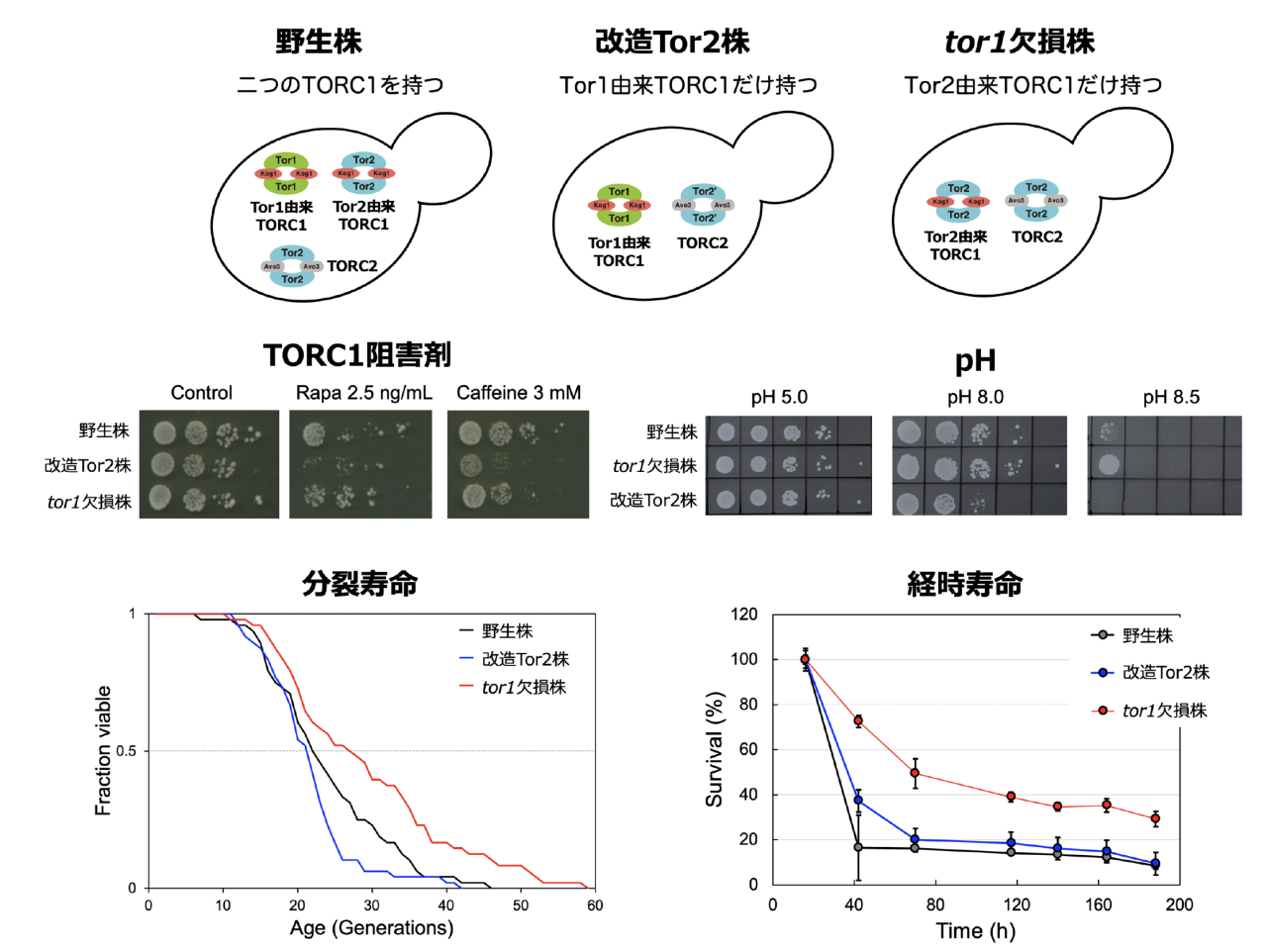
実際にそれらを比較すると、驚くことに二つのTORC1が異なる役割を持つことが明らかになってきました(図3)。TORC1の阻害剤(rapamycin)に対する細胞の感受性やpH環境の違いによる細胞の生育、さらには細胞の寿命までも異なっていることが明らかになりました。これらの結果は、さまざまな細胞の機能に対して、二つのTORC1が異なる働きをしていることを示しています。そして、今回明らかになった特徴から、Tor1由来のTORC1の方が、他の生物種に一種類しか存在しないTORC1と同じような働きをしている、つまりTor2由来のTORC1は出芽酵母特有のものであることも示唆されました。
今後の展開・この研究の社会的意義
本研究では、予測構造モデルに基づいてタンパク質を改造することが、細胞生物学の研究に貢献できることが示されました。近年、機械学習を用いた高精度なタンパク質構造予測プログラムの出現により、信頼性の高いタンパク質構造が気軽に得られるようになったと言われています。今後ますます同様なアプローチの研究が増え、タンパク質構造予測およびタンパク質の合理的改造技術が生物学研究に役立つことが期待されます。
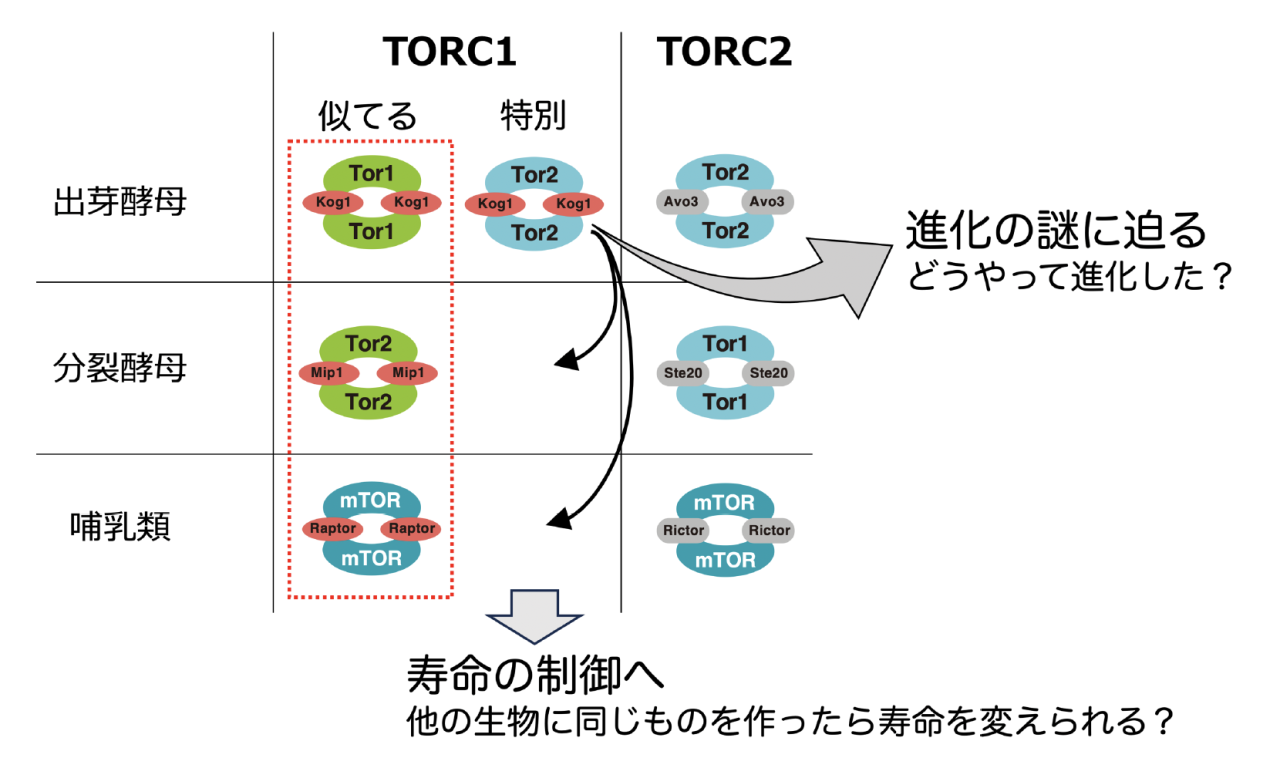
予測構造モデルに基づくタンパク質改造技術を利用した本研究により、出芽酵母の二つのTORC1が異なる働きをしていることが示されました。今回解析を行った出芽酵母は2種類のTORC1を持ちますが、ヒトを含む哺乳類など1種類のTORC1しか持たない生物種も多く存在します。TORC1の分子進化については多くの謎が残されていますが、本研究は、その謎を解き明かす上でも大きな意味を持つと考えられます。出芽酵母のTor2はTORC1にもTORC2にもなることができることから、もともとTor2に対応するものが存在し、進化の過程でTORC1だけになることができるTor1が後から出現したと考えることができます。しかしながら、今回の結果からは、Tor2由来のTORC1が出芽酵母特有のものであることが示唆されました。これは、TORC1がどのように進化してきたのか新たな情報を与えるものとなり、この結果が今後の分子進化を研究する際に大いに役立つと考えられます(図4)。
寿命に関してもTor1由来のTORC1がヒトなどのTORC1と同じ働きをしており、Tor2由来のTORC1は寿命に関して大きな影響がないことが示唆されました。今後、これら酵母の二つのTORC1の機能をより詳細に調べ、それらの機能のバランスを制御することができるようになれば、寿命をコントロールすることも可能になると考えられます。さらに、本研究を発展させることで、ヒトの寿命研究にも貢献できると考えられます。分裂酵母やヒトを含む哺乳類に存在しない出芽酵母Tor2由来のTORC1と同じような働きを持つものをヒトの中に作り出すことで、寿命の延長を実現できるといった可能性も期待されます(図4)。
用語解説
(1)トア(TOR, Target of Rapamycin)複合体
トアは真核生物に高度に保存されたSer/Thrプロテインキナーゼ(リン酸化酵素)であり、数種のタンパク質と2種類の独立したトア複合体1,2(TORC1, TORC2)を形成する。細胞の環境への応答に不可欠であり細胞寿命にも関わっている。
(2)出芽酵母
出芽酵母は研究室でよく用いられる一種の微生物。パンを膨らませる酵母と同じ種類で、「出芽」と呼ばれる、細胞が膨らみ小さな突起を作る方法で新しい細胞を作り出す。生物学の基本的なメカニズムを理解するためのモデル生物として重宝されている。
(3)キナーゼ
キナーゼは、細胞の機能調節に重要な酵素(タンパク質)の一種。キナーゼはターゲットとなるタンパク質にリン酸を付加することで、「スイッチ」のオンオフのように、タンパク質の活性を制御することが出来る。リン酸化は、タンパク質の活性を制御する重要な手段であり、キナーゼは多くの生命現象の制御において中心的な役割を果たす。
(4)遺伝子を欠損させる
特定の遺伝子の機能を意図的に失わせる手法。この手法により、その遺伝子が生体内でどのような働きをしているかを解明することができ、病気の研究や治療法の開発に役立てられている。
論文情報
掲載誌:Journal of Cell Science
論文タイトル:Structure-based engineering of Tor complexes reveals that two types of yeast TORC1 produce distinct phenotypes(トア複合体を改造することで酵母の2種類のTORC1が異なる表現型を生み出していることを明らかにした)
著者:Yoshiaki Kamada*, Chiharu Umeda, Yukio Mukai, Hokuto Ohtsuka,
Yoko Otsubo, Akira Yamashita, and Takahiro Kosugi*
掲載日:2024年2月28日(オンライン公開)
DOI:https://doi.org/10.1242/jcs.261625
研究グループ
自然科学研究機構 分子科学研究所
自然科学研究機構 生命創成探究センター(ExCELLS)
総合研究大学院大学
自然科学研究機構 基礎生物学研究所
長浜バイオ大学
名古屋大学
研究サポート
本研究は、大学共同利用機関法人自然科学研究機構若手研究者による分野間連携研究プロジェクト(01312108)、大学共同利用機関法人自然科学研究機構分野融合型共同研究事業(01112205)、JST戦略的創造研究推進事業さきがけ(JPMJPR20E6)、科学研究費補助金(JP21K05363)などの支援を受けて実施されました。
研究に関するお問い合わせ先
小杉 貴洋(こすぎ たかひろ)
自然科学研究機構 分子科学研究所/生命創成探究センター/総合研究大学院大学、助教
TEL:0564-55-7379、0564-55-7382
E-mail:takahirokosugi@ims.ac.jp
鎌田 芳彰(かまだ よしあき)
自然科学研究機構 基礎生物学研究所/総合研究大学院大学、助教
TEL:0564-55-7536
E-mail:yoshikam@nibb.ac.jp
報道担当
自然科学研究機構 分子科学研究所 研究力強化戦略室 広報担当
TEL:0564-55-7209 FAX:0564-55-7340
E-mail:press@ims.ac.jp
自然科学研究機構 基礎生物学研究所 広報室
TEL:0564-55-7628 FAX:0564-55-7597
E-mail:press@nibb.ac.jp
自然科学研究機構 生命創成探究センター 研究戦略室
TEL:0564-59-5203 FAX:0564-59-5202
E-mail:press@excells.orion.ac.jp
総合研究大学院大学 総合企画課 広報社会連携係
TEL:046-858-1629
E-mail:kouhou1@ml.soken.ac.jp
長浜バイオ大学 アドミッション・オフィス 広報担当
TEL:0749-64-8100 FAX:0749-64-8140
E-mail:kouhou@nagahama-i-bio.ac.jp
プレスリリース
同じだと考えられていた2種のトア複合体は異なる役割を持っていた 〜複合体の構造を予測し合理的に改造することで発見〜
メディア掲載情報
■360doc个人图书馆
[2024年3月2日] 掲載記事

