東京大学物性研究所の井上 圭一 准教授と名古屋工業大学大学院工学研究科およびオプトバイオテクノロジー研究センターの神取 秀樹 教授、角田 聡 客員准教授、名古屋大学(兼・自然科学研究機構生命創成探究センター(ExCELLS))の内橋 貴之 教授、自然科学研究機構生命創成探究センター(ExCELLS)の渡辺 大輝 特任助教(研究当時)、イスラエル工科大学のオデド・ベジャ 教授、チェコ科学アカデミーのロヒット・ガイ博士らの国際共同研究グループは、全ての真核生物の祖先に近いとされるアスガルド古細菌の持つシゾロドプシンと呼ばれるタンパク質が、光エネルギーを使って細胞内へ水素イオンを取り込む機能を持つ分子であることを初めて明らかにしました。
本成果は、アスガルド古細菌が真核生物への進化の過程において、太陽光と酸素のある環境へ進出する際に、独自の光駆動型の内向き水素イオンポンプ(注3)ロドプシンを持つようになったことを示唆しています。
また今後は脳の神経細胞が関連するうつ病などの発病メカニズム研究や、血液の酸性化に伴う、細胞疾患であるアシドーシスなどの機構解明に向けた分子ツールとして、シゾロドプシンの医学研究への応用も期待されます。
本研究成果は、4月10日(日本時間4月11日)に米国科学雑誌「Science Advances」(オンライン版)に公開されます。
なお、本研究成果はEurekAlert!及びAlphaGalileoでも紹介されました。[2020.4.13]
EurekAlert!: Light driven proton pump in distant relative
AlphaGalileo: Light driven proton pump in distant relative – Unique protein acts as an inward proton pump in a distant microbial relative
本研究成果のポイント
- 私たちヒトを含む、全ての真核生物の祖先に最も近縁なアスガルド古細菌が持つ、シゾロドプシンと呼ばれるタンパク質が、光のエネルギーを使って細胞内に水素イオン(H+)を輸送する機能を持つことを明らかにしました。
- 他のロドプシン(注1)類には見られない、シゾロドプシンがもつ光エネルギーを使って水素イオンを輸送するための巧妙な分子機構を明らかにしました。
- 本研究は、アスガルド古細菌が真核生物へと変化する過程で、太陽光や酸素のある環境に順応するために、シゾロドプシンによる水素イオンの取込みが関わっていたという、新たな生物学的理解を深めるものであり、また今後は、シゾロドプシンが脳神経疾患やアシドーシス(注2)などの疾患研究のための分子ツールとなることが期待されます。
研究の背景
私たちヒトを含む動物や植物などは、細胞の中に遺伝情報をコードしたDNAを包む核を持ち、真核生物と呼ばれています。一方で、大腸菌など原始的な生物は細胞内に核を持たず、原核生物と呼ばれています。生物の歴史上、どのようにして原核生物から進化して、真核生物が生まれたのかはいまだに大きな謎とされています。
その中で、近年アスガルド古細菌と呼ばれるグループの原核生物が、ゲノム配列の比較から真核生物に最も近い種であることが明らかになってきました。しかし、一般にアスガルド古細菌は光や酸素の無い海底や湖底の泥の中に棲息していることから、どのようにして多くの真核生物が棲む、光や酸素のある環境に進出できたのか、その進化的なプロセスが不明でした(図1)。
2019年初め、本研究グループがルーマニアから新たに発見されたアスガルド古細菌の遺伝子情報を調べたところ、光のエネルギーを使ってさまざまな生理機能を発揮するロドプシンの中で、これまでにないタイプのものをこれらのアスガルド古細菌が持つことが明らかになりました(Bulzu et al., Nat. Microbiol. 4, 1129-1137 (2019).)。この新しいタイプのロドプシンはシゾロドプシンと名付けられましたが、具体的に光でどのような機能を発現するのか明らかになっておらず、アスガルド古細菌が一体何のためにシゾロドプシンを使って光を利用しているのかはよくわかっていませんでした。
研究の内容
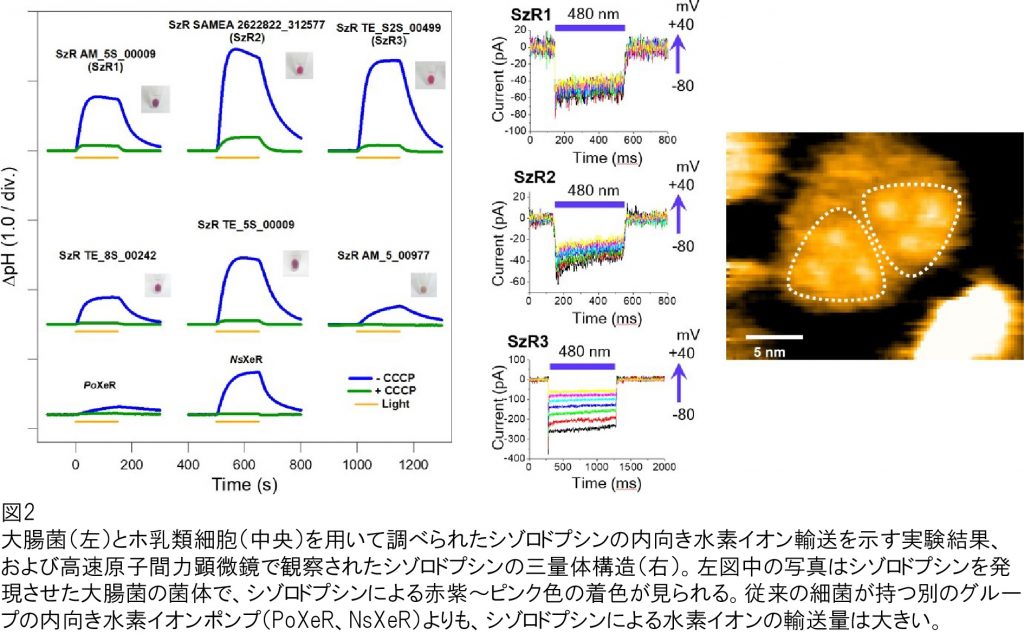
今回、本研究グループはシゾロドプシンの機能を調べるため、大腸菌やホ乳類の細胞にその遺伝子を導入し、タンパク質を大量に発現させることを試みました。その結果大腸菌の細胞中に大量のシゾロドプシンを発現させることに成功しました。そしてその機能を解析したところ光を照射すると細胞内に水素イオンを輸送する、内向き水素イオンポンプ機能を持つことが明らかとなりました(図2左、中央)。このような光で細胞内に水素イオンを輸送するロドプシンは、近年深海などで見つかった、古細菌とは進化的に遠く離れた一部の細菌でのみ知られていましたが、この発見により真核生物に進化する直前のアスガルド古細菌も光を使って細胞内に水素イオンを取り込んでいることが初めて示唆されました。またさらにシゾロドプシンは海洋に広範に棲む未知の微生物グループにもあることが本研究の中で見いだされました。
次に、研究グループはシゾロドプシンがどのようにして光エネルギーを使って、細胞内へ水素イオンを運ぶのか、そのメカニズムを明らかにするために、タンパク質を精製してその性質を詳細に調べました。その結果アスガルド古細菌のシゾロドプシンは、主に557ナノメートル(注4)の光を、海洋性微生物のものは542ナノメートルの光を吸収することが示され、棲息する環境や生物種によって利用する光の波長(色)が異なることが示唆されました。またさらに分子全体の構造を高速原子間力顕微鏡(注5)で観察したところ、同一の3つの分子が集まった三量体構造を持つことが明らかになりました(図2右)。
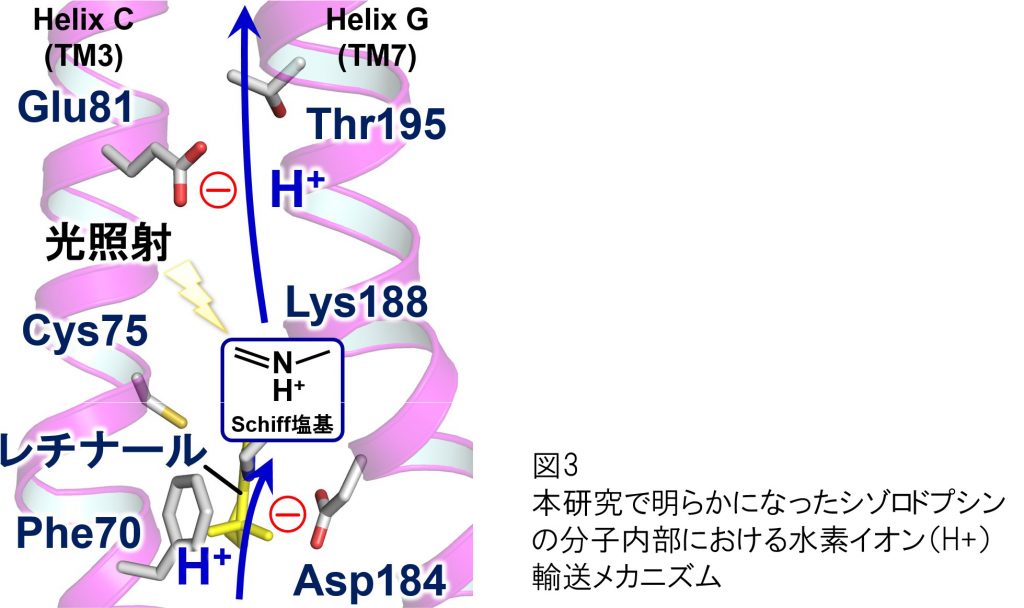
さらに、光を吸収した際にタンパク質の中で起こる反応や分子構造変化を、ナノ秒レーザーを用いた高速分光計測や高精度の赤外分光(注6)計測で解析したところ、シゾロドプシンはレチナール(注7)とタンパク質内外の溶媒との間で、水素イオンをやり取りすることで、細胞内へ一方向的に水素イオンを輸送することが明らかになりました(図3)。この際にはタンパク質を構成する複数のアミノ酸がタンパク質内部での水素イオンの移動に関わることが示唆されており、今回の研究では少なくとも4つのアミノ酸が特に重要な役割を持つことが、アミノ酸改変体タンパク質(注8)を用いた実験で明らかにされました。
今後の展望
本研究は、アスガルド古細菌が真核生物への進化の過程において、太陽光と酸素のある環境へ進出する際に、独自の光駆動型の内向き水素イオンポンプロドプシンを持つようになったことを示唆しており、今後は、本来のアスガルド古細菌の中で細胞の内向き水素イオン輸送がどのような役割を果たすのか、その解明に向けた研究が必要になると考えられます。
また本研究で明らかになったシゾロドプシンの輸送メカニズムは、ヒトなどの体内に存在するイオン輸送タンパク質が、どのようにして輸送するイオンの種類や方向を決定するのかという大きな問題に新たな知見を与えるものであり、他のタンパク質の分子メカニズムの理解へつながると期待されます。また、脳の神経細胞が関連するうつ病などの発病メカニズムの研究や、血液の酸性化に伴う、細胞疾患であるアシドーシスなどの機構解明に向けた分子ツールとして、シゾロドプシンの医学研究への応用も期待されます。
用語解説
(注1)ロドプシン
動物から細菌などの微生物まで、幅広い生物種の細胞膜上に存在する太陽光を吸収してさまざまな生物学的機能を発現するタンパク質。動物の持つロドプシンは視覚など光に関わるシグナル伝達を行う受容体であるのに対し、微生物の持つロドプシンの多くは光のエネルギーを使ってイオンを輸送する。従ってその機能は互いに大きく異なり、進化的にも全く別系統であるにも関わらず、光を吸収するために共にビタミンAの誘導体であるレチナール色素をタンパク質内部に結合し、7本の膜を貫通するらせん(ヘリックス)からなるタンパク質構造を持つなど多くの共通点がある。
(注2)アシドーシス
ヒトの血液は通常中性付近に保持されているが、何らかの原因で血液が酸性化する疾患。酸性化すると血中に大量の水素イオンが生じ、組織や細胞へ障害をもたらすことがある。
(注3)イオンポンプ
ヒトを含めあらゆる生物が持つ細胞内外にイオンを輸送する機能を持つタンパク質であり、多くの創薬開発においてターゲットとされている。イオンポンプはさまざまなエネルギーを使ってイオンを濃度勾配に逆らって輸送する機能を持つが、微生物の持つロドプシンの多くは光のエネルギーを用いて輸送を行うイオンポンプの一種に分類される。
(注4)ナノメートル
1ナノメートル(1nm)は、10億分の1メートルに対応する。光の波長の単位にも使われる。
(注5)原子間力顕微鏡
ナノメートルレベルの鋭い先端を持つ探針をタンパク質などの試料表面に近づけ、その間にはたらく力を測定することで、試料表面の凹凸を可視化する顕微鏡。
(注6)赤外分光
赤外光はヒトの目で見ることのできる可視光より長く、電磁波より短い波長域に波長を持つ光の総称である。赤外分光ではさまざまな波長の赤外光の試料による吸収の強さを見ることで、分子の構造や分子間相互作用の強さなどを調べることができ、特に試料がタンパク質の場合はタンパク質を構成するアミノ酸の微少な構造の違いを見分けることができる。
(注7)レチナール
通常アミノ酸は可視領域に吸収を持たないため、アミノ酸で構成されるタンパク質もそれ単体では可視光を利用することができない。それに対してロドプシンはタンパク質内部に、体内の酵素反応でビタミンAから生じるレチナールと呼ばれる色素を結合している。ロドプシンのタンパク質内部にあるレチナールが可視光を吸収するとその構造が変化し、それを通じてタンパク質部分にも変化が起こり、さまざまな生理機能を発現することが可能になる。
(注8)アミノ酸改変体タンパク質
ロドプシンのタンパク質はおよそ200個程度のアミノ酸から構成されているが、遺伝子工学的な手法を用いることで、タンパク質上の任意の場所にあるアミノ酸を本来とは別の種類(アミノ酸は一般に20種類が生物の体内に存在する)のアミノ酸へと置き換えることができる。このように作製されるのがアミノ酸改変体タンパク質であり、その機能や物性を見ることで、本体のタンパク質において、それぞれのアミノ酸がどの様な役割を持つのかを調べることができる。
発表者
井上 圭一(東京大学物性研究所 准教授)
神取 秀樹(名古屋工業大学 大学院工学研究科、オプトバイオテクノロジー研究センター 教授)
角田 聡(名古屋工業大学 大学院工学研究科、オプトバイオテクノロジー研究センター 特任准教授)
内橋 貴之(名古屋大学 教授 兼・自然科学研究機構 生命創成探究センター(ExCELLS)客員教授)
渡辺 大輝(研究当時:自然科学研究機構 生命創成探究センター(ExCELLS)特任助教)
研究サポート
本研究は、日本学術振興会(JSPS) 科学研究費助成事業、科学技術振興機構(JST) 戦略的創造研究推進事業(さきがけ「新規光受容タンパク質が先導する新しいオプトジェネティクス(研究者: 井上 圭一)」、CREST「細胞内二次メッセンジャーの光操作開発と応用(研究代表者: 神取 秀樹)」、さきがけ「新規酵素型ロドプシンを用いた視覚再生の挑戦(研究者: 角田 聡)」)による支援を受けて行われました。
掲載論文
雑誌名
「Science Advances」(オンライン版)
掲載日
2020年4月10日(日本時間 2020年4月11日)
論文タイトル
Schizorhodopsins: A family of rhodopsins from Asgard archaea that function as light-driven inward H+ pumps
著者
Keiichi Inoue, Satoshi P. Tsunoda, Manish Singh, Sahoko Tomida, Shoko Hososhima, Masae Konno, Ryoko Nakamura, Hiroki Watanabe, Paul-Adrian Bulzu, Horia L. Banciu, Adrian-Ştefan Andrei, Takayuki Uchihashi, Rohit Ghai, Oded Béjà, Hideki Kandori.
DOI
10.1126/sciadv.aaz2441
本件に関するお問い合わせ先
研究全般に関するお問い合わせ先
東京大学物性研究所
准教授 井上 圭一(いのうえ けいいち)
TEL: 04-7136-3230
E-mail: inoue_at_issp.u-tokyo.ac.jp ※_at_は@にご変更ください。
名古屋工業大学大学院工学研究科 生命・応用化学専攻
オプトバイオテクノロジー研究センター
教授 神取 秀樹(かんどり ひでき)
TEL: 052-735-5207
E-mail: kandori_at_nitech.ac.jp ※_at_は@にご変更ください。
名古屋大学大学院理学研究科
教授 内橋 貴之(うちはし たかゆき)
TEL: 052-789-2885
E-mail: uchihast_at_d.phys.nagoya-u.ac.jp ※_at_は@にご変更ください。
JST事業に関すること
科学技術振興機構 戦略研究推進部 グリーンイノベーショングループ
嶋林 ゆう子(しまばやし ゆうこ)
TEL: 03-3512-3531
Fax: 03-3222-2066
E-mail: presto_at_jst.go.jp ※_at_は@にご変更ください。
報道に関するお問い合わせ先
東京大学物性研究所 広報室
TEL: 04-7136-3207
E-mail: press_at_issp.u-tokyo.ac.jp ※_at_は@にご変更ください。
名古屋工業大学 企画広報課
TEL: 052-735-5647
Fax: 052-735-5009
E-mail: pr_at_adm.nitech.ac.jp ※_at_は@にご変更ください。
名古屋大学総務部総務課広報室
TEL: 052-789-2699
Fax: 052-789-2019
E-mail: nu_research_at_adm.nagoya-u.ac.jp ※_at_は@にご変更ください。
自然科学研究機構 生命創成探究センター 広報担当
TEL: 0564-59-5201
Fax: 0564-59-5202
E-mail: press_at_excells.orion.ac.jp ※_at_は@にご変更ください。
科学技術振興機構 広報課
TEL: 03-5214-8404
Fax: 03-5214-8432
E-mail: jstkoho_at_jst.go.jp ※_at_は@にご変更ください。