分子科学研究所 協奏分子システム研究センター/生命創成探究センター 生命分子創成研究グループの古賀信康准教授、古賀理恵特任研究員、Nexomics Biosciences, Inc.のGaohua Liu博士、レンセラー工科大学のGaetano T. Montelione教授、ワシントン大学のJavier Castellanos博士課程学生(当時)、David Baker教授の研究グループは、100残基を超えるαβ型タンパク質構造の人工設計において、3次構造全体における主鎖構造の歪みを考慮する必要性があることを発見しました。この研究成果により、従来よりもより大きく複雑な人工タンパク質の設計が可能になり、機能性タンパク質の創出につながる可能性が期待されます。
本研究成果は、学術誌「Nature Communications」に2021年6月24日付でオンライン掲載されます。
本研究成果のポイント
- これまでに、局所主鎖構造(2次構造(#1)の長さやループの形状)と形成しやすい超2次構造(#1)に関するルールを基にタンパク質構造設計原理を構築し、これを用いることで4本のβストランドからなるβシートと、複数のαヘリックスを持つ100残基程度のαβ型タンパク質の設計に成功してきた
- 機能を持つタンパク質を創出するためには、機能部位を埋め込むために、より多くのαヘリックスやβストランドで構成される大きく複雑なタンパク質構造を自在に設計できる技術が重要
- しかし、構築した設計原理を用いて、100残基を超える5本または6本のβストランドからなるβシートを持つαβ型タンパク質構造の人工設計を試みると、設計したタンパク質は設計構造とは異なるストランドの並びを持った3次構造(#1)に折り畳んだ
- 設計と異なる構造に折り畳んだ原因を調べた結果、大きく複雑なタンパク質構造の人工設計には、これまでに構築した設計原理に加えて、3次構造全体における主鎖構造の歪みを考慮する必要があることを突き止めた
- 主鎖構造の歪みを考慮したタンパク質構造設計原理を構築し、これを用いることで5本または6本のβストランドからなるβシートを持つαβ型タンパク質の人工設計に成功した
研究の背景
タンパク質の人工設計技術は、近年、飛躍的な発展を遂げています。その発展を支えたのは、研究グループの構築した局所主鎖構造と形成しやすい超2次構造に関するルールを基にしたタンパク質構造設計原理です。研究グループはこれまでに、構築した原理を用いることで、100残基以下の様々な形状のタンパク質構造の創出に成功してきました。そこで研究グループは、このタンパク質構造設計原理が、より大きく複雑なタンパク質構造の人工設計にも適用できるのか、5本および6本ストランドからなる100残基以上のサイズのαβ型タンパク質構造の人工設計を行いました。しかし、核磁気共鳴分光法(#2)により決定された実験構造は、計算機で設計した構造と異なり、内部のストランドの並びが入れ替わっていました(図1)。
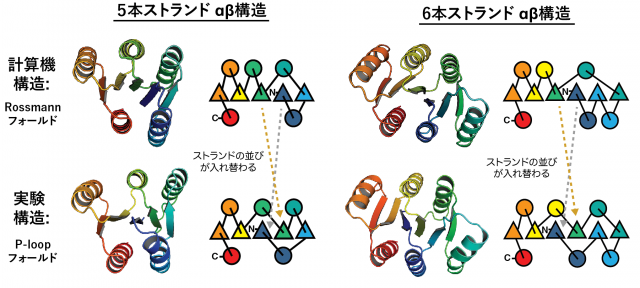
研究の成果
研究グループは、この問題を解決するために、様々な仮説を立て研究を行ってきました。その結果、計算機で設計した構造を構築するために用いた設計図は、実験構造から復元した設計図と比べて、タンパク質構造全体にわたる主鎖構造の歪みを生じるために、「βシート形成度」および「両末端ヘリックス間のパッキング度」が低いことを、折り畳みシミュレーションにより明らかにしました(図2)。さらに研究グループは、ストランドの長さを短くすることや、βストランド間の相対的な位置を調整することで、主鎖構造の歪みを抑えながら、βシート形成および両末端ヘリックス間のパッキング度合いを高められることを明らかにしました(図3)。
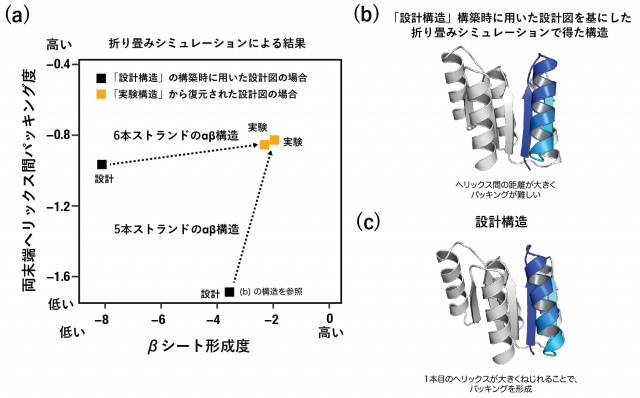
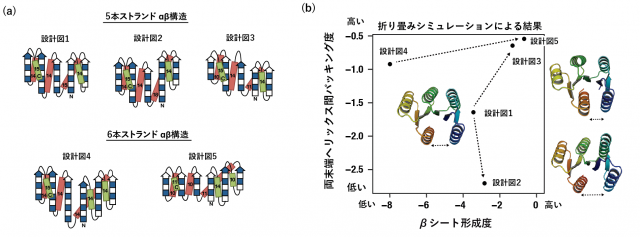
次に研究グループは、これらの発見を基に、5本および6本ストランドからなる100残基以上のサイズのαβ型タンパク質構造の人工設計を試みました。「βシート形成度」および「両末端ヘリックス間パッキング度」が高くなるような、主鎖構造歪みの低い主鎖構造設計図を描き(図3(a)の設計図3と5)、これら設計図を基に計算機により主鎖構造を構築した後に、これら主鎖構造を安定化するようなアミノ酸配列を持つタンパク質を設計しました。設計したタンパク質の実験構造を核磁気共鳴分光法により決定したところ、設計通りのストランドの並びを持つ3次構造に折り畳んでいることが明らかになり、5本および6本ストランドからなるαβ型タンパク質の人工設計に成功しました(図4)。
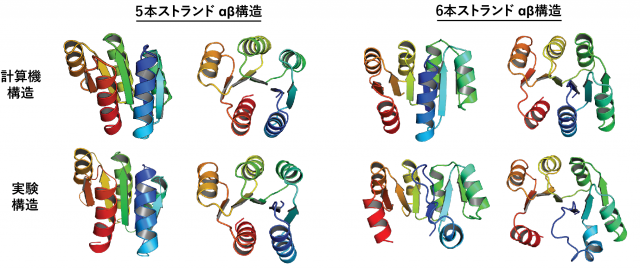
今後の展開・この研究の社会的意義
本研究により、主鎖構造の歪みを考慮することで、従来よりも大きく複雑なタンパク質構造を設計することが可能になりました。大きく複雑なタンパク質構造を新規に人工設計することが可能になれば、その3次構造中に機能部位を構築できる可能性が高まります。本研究により、生命現象の制御・設計、医療等に貢献する新規機能性タンパク質の創成につながることが期待されます。
用語解説
(#1) 2次構造・超2次構造・3次構造(タンパク質の階層構造):
タンパク質は1次から4次の階層構造を持つ。1次構造はアミノ酸の配列、2次構造は連結されたアミノ酸残基の主鎖間の規則的な水素結合で形成される局所的な構造(αヘリックス、βシートなど)、超2次構造は数個の2次構造が組み合わさって特異的に形成される構造、3次構造は超2次構造が側鎖間のパッキング等の非共有結合的な相互作用で組み合わさって形成される構造、4次構造は複数のタンパク質分子が集まって形成される構造である。
(#2) 核磁気共鳴分光法:
タンパク質を磁場中に置きラジオ波を照射することで生じる核スピンの共鳴現象を観測することにより、タンパク質の分子構造を原子レベルで解析することができる。
(#3) フォールド:
タンパク質の形を、αヘリックスやβシートなどの2次構造要素の空間における並びと、そのつながりで定義したもの。
論文情報
掲載誌:Nature Communications
論文タイトル:“Role of backbone strain in de novo design of complex α/β protein structures”
(「複雑なα/β型タンパク質構造の人工設計における主鎖構造歪みの重要性」)
著者:Nobuyasu Koga*, Rie Koga, Gaohua Liu, Javier Castellanos, Gaetano T. Montelione*, and David Baker*(*責任著者)
DOI:10.1038/s41467-021-24050-7
研究グループ
分子科学研究所/生命創成探究センター
ワシントン大学
Nexomics Biosciences, Inc.
レンセラー工科大学
研究サポート
科研費・若手研究(A) 15H05592(古賀信康)
新学術・発動分子科学 18H05420(古賀信康)
科学技術振興機構 さきがけ JPMJPR13AD(古賀信康)
科研費・海外特別研究員(古賀信康)
HHMI, DOE, DARPA, DTRA, NIH R01-GM120574
本件に関するお問い合わせ先
研究について
分子科学研究所/生命創成探究センター
准教授 古賀 信康(こが のぶやす)
TEL:0564-55-7379
E-mail:nkoga_at_ims.ac.jp
※_at_は@にご変更ください。
報道について
自然科学研究機構 分子科学研究所 研究力強化戦略室 広報担当
TEL:0564-55-7209 FAX:0564-55-7374
E-mail:press_at_ims.ac.jp
※_at_は@にご変更ください。

