概要
自然科学研究機構 生命創成探究センター/生理学研究所の村田和義 特任教授の研究グループは、ウプサラ大学の岡本健太 主任研究員、エクス=マルセイユ大学のChantal Abergel教授と共同で、巨大ウイルスの一種であるメルボルンウイルスのカプシド(外殻)構造を、クライオ電子顕微鏡法により4.4 Å(オングストローム)分解能で明らかにすることに世界で初めて成功しました。本研究では、電子顕微鏡画像の解析に「ブロック型再構成法」を応用することで、三次元再構成像の分解能を飛躍的に向上させることに成功しました。その結果、巨大なカプシド(直径250 nm(ナノメートル))を構成するタンパク質の詳細な配置を明らかにしました。本成果は、限られた種類のタンパク質の組み合わせによって巨大で均一かつ強固な構造体が形成される基本原理の解明に貢献するものです。さらに、ウイルスの進化や感染機構の理解を深めるだけでなく、包摂化合物やドラッグデリバリー担体の設計への応用も期待されます。
本研究成果は、日本時間 2026年4月2日に、国際科学雑誌「Viruses」にオンライン公開されました。
発表のポイント
- 巨大ウイルス「メルボルンウイルス」の外殻(カプシド)構造を、クライオ電子顕微鏡法に「ブロック型再構成法」を応用することにより高分解能で解明した。
- 巨大なカプシド(直径250 nm(ナノメートル))を構成するタンパク質の詳細な配置を解明した。
- 限られた種類のタンパク質の組み合わせによって巨大で均一かつ強固な構造体が形成される基本原理の解明に貢献した。
- ウイルスの進化や感染機構の理解を深めるだけでなく、包摂化合物やドラッグデリバリー担体の設計への応用も期待される。
研究の詳しい内容
1. 背景
巨大ウイルスは、通常のウイルス(直径100 nm※1以下)よりもはるかに大きく、複雑な構造とゲノムを持つことから、生命進化の理解において重要な研究対象と考えられています。その中でもマルセイユウイルス科に属するウイルスは、世界中の環境から発見されていますが、その構造の詳細、特にカプシド内部の構築原理は十分に解明されていませんでした。
マルセイユウイルス科ウイルスは、アメーバに感染する巨大ウイルスで、約360 kbpの大規模なDNAゲノムと直径約250 nmの正二十面体カプシドを特徴とします。2009年の発見以降、複数の系統に分類される多様なメンバーが同定されています。その1種のメルボルンウイルスは2014年にオーストラリアで単離されたウイルスで、従来のクライオ電子顕微鏡法※2により基本的な構造や形態的特徴(五回対称軸での内膜の突出など)は示されていたものの、分解能は十分ではなく詳細な分子構造の理解には至っていませんでした。
近年、巨大ウイルスのクライオ電子顕微鏡法を用いた高分解能構造解析では、ウイルス粒子内で起こるピントのズレの影響を低減し、分解能を向上させる手法「ブロック型再構成法※3」が確立されてきました。この手法により、巨大なウイルスでも主要カプシドタンパク質(MCP)や複数の副カプシドタンパク質(mCP)の原子モデル構築が可能となってきました。
本研究では、この「ブロック型再構成法」をメルボルンウイルスの構造解析に応用することで、巨大なカプシドを構成するタンパク質の詳細な配置を解明しました。
2. 本研究の内容と成果
本研究では、クライオ電子顕微鏡法にブロック型再構成法を応用することで、メルボルンウイルスのカプシド構造を4.42 Å※1の高分解能で解析しました(図1)。その結果、MCPおよびそれを支えるmCPの配置や相互作用が明らかとなり、カプシド形成に関わる分子ネットワークの詳細が示されました(図2)。
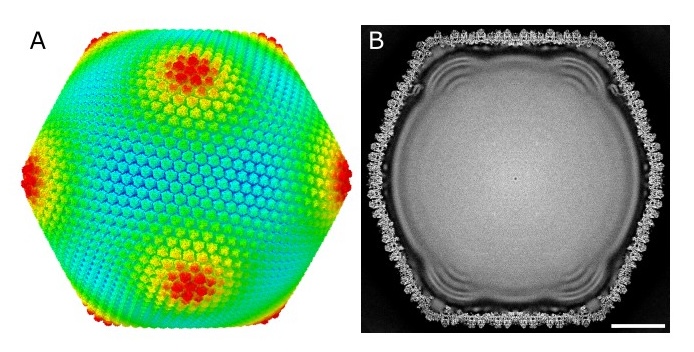
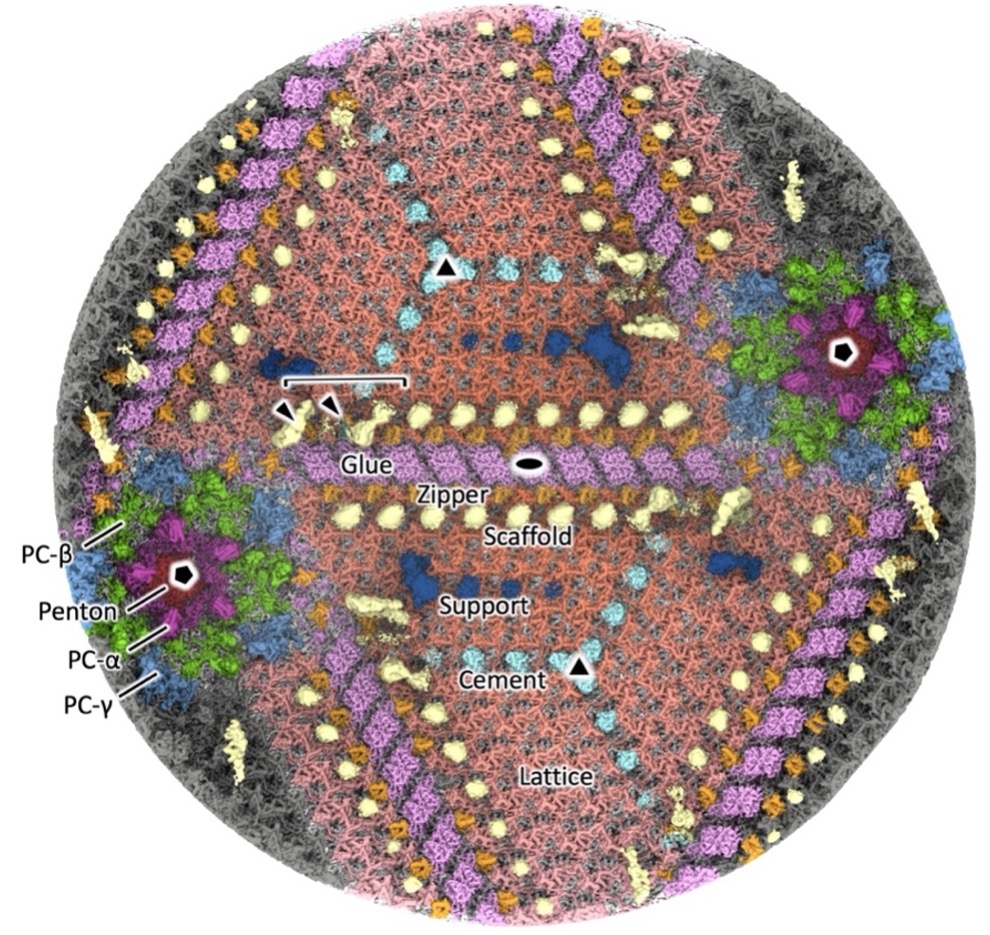
メルボルンウイルスの正二十面体カプシドは、表面が他の巨大ウイルスと同様に単一のMCPで覆われている一方で、これを支えるmCPは、複数のタンパク質から構成され、本ウイルスが属するマルセイユウイルス科ウイルス独自の分子ネットワークを形成していることが明らかになりました(図2)。正二十面体カプシドの12か所の五角形をした頂点は、Penton、PC-α、PC-β、PC-γと名付けられたタンパク質群によって構成されていました。また、これらの頂点の間に配置された20個の三角形をした領域は、Cement、Lattice、Supportと呼ばれるタンパク質群からなり、それぞれがGlueおよびZipperと呼ばれるタンパク質群によって連結されていました。
さらに、カプシド内側にはScaffold(足場)と名付けられたタンパク質群が接合部に沿って配置されており、カプシドの内側から構造の安定化や形成に寄与していることが示唆されました。これらの結果から、マルセイユウイルス科のウイルスは他の巨大ウイルスと一部共通する基本構造を持ちながらも、Scaffoldタンパク質群などの独自要素によってカプシドのサイズや構築を制御している可能性が示されました。
3.成果の意義と今後の展開
本研究成果は、巨大ウイルスの構造多様性および形成機構の理解を深めるものです。これらの結果は、巨大ウイルスが共通の構造原理を利用しつつも、多様で柔軟な構築戦略を有していることを示しており、そのカプシド形成機構と機能的ネットワークの理解を大きく前進させるものです。さらに、本成果は巨大ウイルスの進化的多様性を示す重要な知見へと発展することも期待されます。加えて、本研究で明らかとなった分子ネットワークの構造原理は、包摂化合物やドラッグデリバリー担体の分子設計への応用にも寄与することが期待されます。
4. 用語説明
※1:Å(オングストローム)、nm(ナノメートル)
長さの単位。1 Åは0.1 nmで水素原子1個の大きさに相当。1 nmは0.000001mm。
※2:クライオ電子顕微鏡法
生物試料を低温(約-170℃)で観察することができる電子顕微鏡。生物試料を水溶液環境中で凍結させて、そのまま観察することができる。
※3:ブロック型再構成法
試料をいくつかのブロックに分割して、独立に三次元再構成する方法。
Zhu et al. Pushing the Resolution Limit by Correcting the Ewald Sphere Effect in Single-Particle Cryo-EM Reconstructions. Nat. Commun. 2018, 9, 1552.
研究助成等について
本研究は、科学研究費補助金(JP19H04845)、AMED BINDS(JP24ama121005, JP25ama121005)、スウェーデン研究評議会、スウェーデン研究・高等教育国際協力財団、スウェーデン王立科学アカデミー等の支援を受けて行われました。
論文情報
- 雑誌名:Viruses
- 論文名:
The 4.4 Å Capsid Structure of the Giant Melbournevirus Belonging to the Marseilleviridae Family - 著者:Raymond N. Burton-Smith, Chantal Abergel, Kenta Okamoto, Kazuyoshi Murata*
(*責任著者)
- 論文公開日:2026年4月2日
- 掲載URL:https://www.mdpi.com/1999-4915/18/4/433
- DOI:10.3390/v18040433
著者情報
Raymond N. Burton-Smith、村田 和義(生命創成探究センター/生理学研究所)、岡本 健太(ウプサラ大学)、Chantal Abergel(エクス=マルセイユ大学)
お問い合わせ先
研究内容に関するお問い合わせ
自然科学研究機構 生命創成探究センター/生理学研究所
特任教授 村田 和義
E-mail:kazum_at_nips.ac.jp
広報に関するお問い合わせ
自然科学研究機構 生命創成探究センター(ExCELLS)研究力強化戦略室
E-mail:press_at_excells.orion.ac.jp
自然科学研究機構 生理学研究所
E-mail:pub-adm_at_nips.ac.jp
※_at_を@に変換してください。
プレスリリース
巨大ウイルスの構造を原子レベルで解明
〜 メルボルンウイルスのカプシド構造を4.4 Å分解能で可視化 〜

