研究の概要
大学共同利用機関法人 自然科学研究機構 生命創成探究センター (ExCELLS) のクリスチアン・ガンサー特任助教、西口茂孝特任研究員 (現職: 国立大学法人 大阪大学 大学院工学研究科 特任助教)、国立大学法人東海国立大学機構 名古屋大学 大学院理学研究科のチャン・フェンユエ研究員、内橋貴之教授(兼ExCELLS客員教授)の研究グループは、これまで困難とされてきた生きた細菌の膜の動的な力学的性質をナノスケールで測定する新しい顕微鏡技術「高速インラインフォースマッピング (HS-iFM) *1」の開発に世界で初めて成功しました。
研究グループは、この技術を用い、モデル生物として知られる大腸菌 (Escherichia coli) の細胞膜の硬さが細胞分裂時にどのように変化するかを、これまでになく詳細に観察しました。細胞の硬さは、薬剤の投与やがん化によって変化することが示唆されており、これらの研究に本技術を適用することで、細菌に対する抗生物質の効果検証や動物細胞のがん化の機構解明につながることが期待されます。
本研究成果は、2025年1月30日に国際科学雑誌 「Science Advances」 にオンライン掲載されました。
発表のポイント
- 生きた細菌の膜の硬さを、ナノメートルレベルの解像度でリアルタイムに測定可能。
- 大腸菌の分裂過程で、分裂部位の膜が周囲より顕著に硬化することを発見。
- 細菌に対する抗生物質の効果検証や動物細胞のがん化の機構解明等、医学・生物学分野の研究開発への幅広い応用が期待される。
研究の詳しい内容
1. 背景
細胞の硬さは、薬剤の投与やがん化によって変化することが示唆されており、その変化をナノメートルレベルの解像度で測定可能な顕微鏡技術の開発が望まれていました。しかし、光学顕微鏡では小さな構造を観察するには限界があり、電子顕微鏡では生物試料を生きた状態で観察出来ません。一方、原子間力顕微鏡 (AFM) は、物質の力学的特性を高解像度で測定可能な技術ですが、従来のAFMでは撮影速度が遅いため、生きた細胞で生じる動的な現象の観察には不向きでした。
2. 本研究の手法と成果
この課題を解決するため、研究グループはAFMの高速化と力学的特性測定を組み合わせたHS-iFMを開発しました。この技術により、生きた細胞の分子レベルの表面形状と力学的特性の同時測定が可能になりました。
研究グループは、モデル生物として広く研究されている大腸菌を対象にHS-iFMを用いた観察を行いました。その結果、細胞分裂が進む際に、分裂部位の膜が周囲よりも顕著に硬化することが確認されました。この硬化は、局所的な膜の張力や細胞壁の厚みの増加が原因と考えられています。研究を主導したクリスチアン・ガンサー特任助教は次のように述べています。
「生きた細菌の観察により、細胞が生命活動の中でどのように変化していくかを直接追跡することが可能になりました。大腸菌はこれまで非常によく研究されてきましたが、そのナノスケールでの動的な力学的変化については謎が多く残されていました。」
また、研究グループは細胞分裂中に2つの娘細胞をつなぐ膜の橋が形成され、最終的に破断する様子も観察しました。この橋の形成と破断には平均242秒を要し、このプロセスを7回確認しました。また、分裂中の細胞では直径100 nm未満の柔らかい領域が観察され、その破裂が細胞の圧力低下と死を引き起こしました。興味深いことに、分裂中の細胞が完全には分離していない状態において、片方の娘細胞の破裂が隣接する娘細胞に圧力低下をもたらしました。
さらに、研究グループは分裂中の大腸菌の細胞膜上に孔が形成され、閉じたり再形成されたりする様子を観察しました。この孔は膜小胞 (外膜小胞) の形成に関連すると考えられており、分裂中の新しい細胞壁付近でその頻度が高まることが知られています。ただし、観察された孔の直径(34.7 nm)は、従来報告されている膜タンパク質複合体の直径 (約8 nm) よりも大きく、さらなる調査が必要とされています。
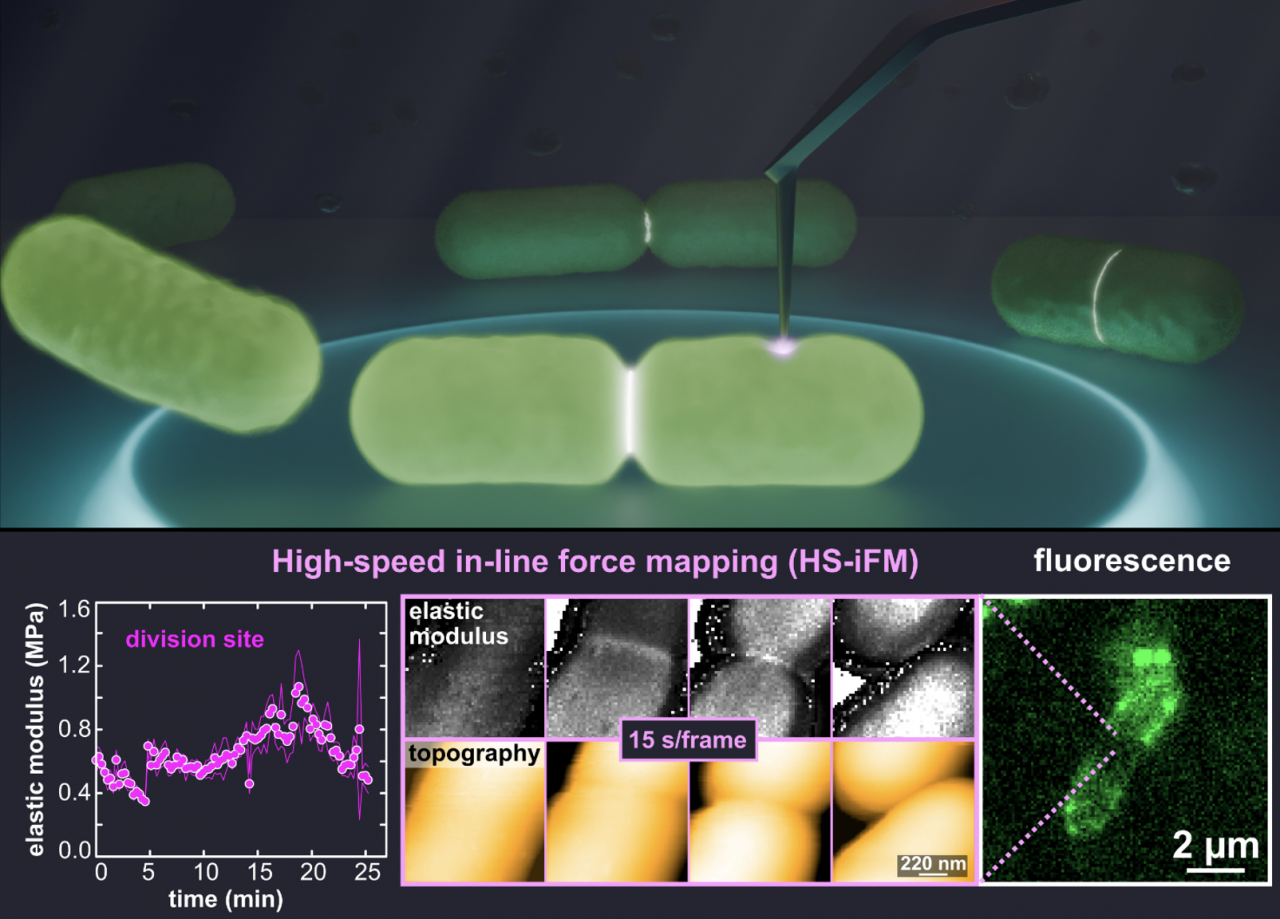
(上図) HS-iFMによる大腸菌の観察のイメージ図. (下図) HS-iFMで計測した大腸菌の硬さ変化のグラフ (左)、HS-iFMで大腸菌を撮影した連続画像 (真ん中)、大腸菌の蛍光画像 (右).
3. 本研究の学術的意義および研究の展望
HS-iFM技術は、大腸菌を含む多様な生物試料の研究を発展させる大きな可能性を秘めています。ガンサー特任助教は次のように述べています。
「今後、抗生物質などの外部刺激が生きた細菌の膜のナノ力学特性に与える局所的かつ動的な影響を研究していきたい。」
研究チームは、HS-iFMを用いて、将来的には個々のタンパク質のような小さな分子の力学的特性を視覚的に観察できるよう、さらなる速度と解像度の向上を目指しています。
4. 研究の社会的意義・社会への波及効果
細胞の硬さは、薬剤の投与やがん化によって変化することが示唆されており、これらの研究にHS-iFMを適用していくことで、細菌に対する抗生物質の効果検証や動物細胞のがん化の機構解明につながることが期待されます。
5. 用語説明
*1 高速インラインフォースマッピング (HS-iFM):先端の直径が数ナノメートルの針を、観察対象物 (タンパク質等) に接触することで、その表面形状と硬さを同時に観察する顕微鏡技術。溶液中において、観察基板に吸着させた観察対象物を高速 (1フレーム/15秒) でスキャンすることにより、表面形状と硬さの変化を高分解能 (表面形状像: 5.5 ナノメートル/ピクセル、硬さ像: 22 ナノメートル/ピクセル) でリアルタイムに画像化することが出来る。
研究助成等について
本研究は、日本学術振興会(JSPS)科研費(JP23H04874、24K01309、22K18943)、科学技術振興機構(JST)CREST(JPMJCR21L2)、文部科学省共同利用・共同研究拠点形成事業(JPMXP1323015482)の支援を受けて実施されました。
論文情報
- 雑誌名:Science Advances
- 論文名:A look beyond topography: transient phenomena of Escherichia coli cell division captured with high-speed in-line force mapping
- 著者:Christian Ganser†*, Shigetaka Nishiguchi†, Feng-Yueh Chan, Takayuki Uchihashi* (†筆頭著者, *責任著者)
- DOI:https://doi.org/10.1126/sciadv.ads3010
お問い合わせ先
研究内容に関するお問い合わせ
自然科学研究機構 生命創成探究センター 客員教授
名古屋大学大学院理学研究科 教授
内橋貴之
E-mail: uchihast_at_d.phys.nagoya-u.ac.jp
広報に関するお問い合わせ
自然科学研究機構 生命創成探究センター 研究戦略室
E-mail: press_at_excells.orion.ac.jp
名古屋大学 総務部広報課
E-mail:nu_research_at_t.mail.nagoya-u.ac.jp
※_at_を@に変換してください。
プレスリリース
生きた大腸菌の膜の“硬さ”を動的に測定する新技術を開発 ー細胞分裂時の膜の硬さを高速・高解像度で観察ー

